I. 서 론
현대에 들어서면서 천연 한방 처방이나 한방에서 사용한 소재의 효능 규명을 통해 기능성 소재를 개발하고 기능성 및 기호도가 증대된 제품 개발을 위한 연구가 꾸준히 진행되고 있다.
한방 생약재를 주성분으로 하는 한방 소재 제품 중 차와 관련된 제품은 황기차, 구기자차, 오가피차, 결명자차 등 종류가 있으나, 대부분 이러한 제품은 단일 한약재를 사용하여 이용하고 있다. 쌍화탕은 여러 종류의 효능이 있는 생약재들을 조합하여 제조하며, 다양한 한약재들에 의해 복합 상승효과를 기대할 수 있는 제품으로 예전부터 건강을 위해 많이 섭취하고 있다. 쌍화탕에 주로 사용되는 한약재는 백작약, 숙지황, 황기, 당귀, 천궁, 계피, 감초, 생강, 대추 등이며, 처음에는 한약으로 처방되었으나 현재는 카페나 가정에서도 쉽게 음료로 애용되고 있다(Park and Lee, 2022).
2000년 이후 쌍화탕의 연구에 대한 분석 결과, 한의학 분야에서 76%로 가장 많았고, 영양학, 약학, 관광경영학 등 여러 학문에서 진행되었으며, 주요 연구분야는 효능평가, 정성분석, 독성, 안전성에 관한 연구가 진행되었다(Nam and Oh, 2019).
쌍화탕은 피로회복과 기혈이 손상되었을 때 사용되는 처방으로 오로(五勞), 육극(六極), 칠상(七傷)에 기혈을 보충하며, 소화작용을 도와 입맛이 살아나며, 허해진 몸을 보하는 약으로 알려져 있다(Kim et al., 2011; Nam and Oh, 2019). 또한, 최근 연구결과에서 따르면 항산화(Kim et al., 2010; Kim et al., 2011), 항피로 효과(Ha and Park, 1998; Park and Park, 1995; Sohn, 1994), 항염(Kim and Hwang, 1981), 간기능 개선(Ann et al., 1984; Cho et al., 1987), 면역(Jung et al., 2010) 등의 효과가 있는 것으로 보고되고 있다. 생산성 증대를 위한 쌍화탕 제조 방법에 관한 연구(Cho, 1995; Kim et al., 2010)와 흡수를 용이하게 하고 효능 증대를 위해 발효한 쌍화탕의 안전성을 확보를 위해 독성실험에 대한 연구도 보고되고 있다(Lee et al., 2009).
쌍화 등의 차는 예전부터 편안한 휴식과 함께 건강을 위해 즐겨 이용하고 있으나, 액상이나 원재료를 끓여서 먹는 불편함이 있다. 이를 개선하여 편하고 쉽게 이용할 수 있는 제품이 티백 형태의 차로 쌍화탕에 사용되는 약재 비율로 티백에 포장된 제품을 열수를 넣고 우려내어 음용할 수 식품유형이다. 기존 티백차 이용 시 침출하는 시간이 쌍화탕을 제조하는 추출 조건에 비해 짧아 용출된 유효성분의 함량이 제한되어 효능이 낮아질 수 있으며, 소비자의 기호도가 좋지 않을 수 있다. 이에 쌍화 추출물을 코팅한 티백차를 제조하여 취급 및 복용이 간단하며, 효능과 기호도가 향상된 제품 개발의 필요성이 있다. 따라서 본 연구는 코팅 쌍화 티백차를 제조하여 효능평가와 관능평가를 통해 상품화 가치를 판단하고자 하였다.
Ⅱ. 재료 및 방법
코팅 상화 티백은 충북약초영농조합법인에서 제조하였다. 쌍화 추출액 액재는 동의보감 처방서인 방약합편(Hwang, 1978)에 기록된 약재와 사용량을 기본으로 하여 백작약 20%, 황기 10%, 당귀 10%, 천궁 10%, 숙지황 5%, 감초 10%, 계피 5%, 대추 10%, 말린 생강 5%, 갈근 5%, 귤껍질 10%의 비율로 배합한 후 100°C에서 2시간 추출한 다음, 여과하여 사용하였다. 쌍화 티백의 원료는 분쇄한 후 동일한 비율로 혼합한 다음 액상 코팅기에 넣고 쌍화 추출액으로 액상 코팅하였다. 액상 코팅된 원료를 100~130°C의 고온에서 50분간 열처리 후 80~90°C의 온도에서 2~4시간 건조기에서 건조한 후 티백기를 이용하여 쌍화 티백을 제조하였다.
코팅하지 않은 쌍화 티백과 액상 분사하여 코팅된 쌍화 티백을 각각 80, 100°C에서 100 mL의 물로 3분간 침지한 후 0.2 μm 시린지 필터(Whatman, USA)로 여과하여 분석용으로 사용하였다.
DPPH 라디칼 소거 활성은 Blois(1958)의 방법을 변형하여 측정하였다. 96 well plate에 0.2 mM DPPH solution 100 μL를 취하고 쌍화 티백 추출액 100 μL를 넣어 섞어 주었다. 시료는 37°C에서 30분간 반응시킨 후 microplate reader(EPOCH, Bio Tek Instruments Inc, USA)를 이용하여 515 nm에서 흡광도 측정하였다. 양성 대조군으로 ascorbic acid 100 μg/mL 농도를 사용하였으며, 대조군은 증류수로 하였다.
SOD 유사활성은 과산화수소(H2O2)로 전환시키는 반응을 촉매하는 pylogallol의 생성량을 측정하여 SOD 유사활성으로 나타내었다. 쌍화 티백 추출액 20 μL에 pH 8.5로 보정한 tris-HCl buffer(50 mM tris [hydroxymethyl] amino-methane, 10 mM EDTA, pH 8.5) 20 μL와 7.2 mM pyrogallol(Sigma- Aldrich, USA) 20 μL를 첨가하여 25°C에 서 10분간 반응시킨 후 1 N HCl 100 μL를 가하여 반응을 정지시켰다. 반응액 중 산화된 pyrogallol의 양은 microplate reader를 사용하여 420 nm에서 흡광도를 측정하였다. SOD 유사활성은 시료 첨가구와 무첨가구 사이의 흡광도 차이를 백분율(%)로 나타내었다.
쌍화 티백의 ABTS 라디칼 소거 활성 측정은 Re 등(1999)의 방법을 변형하여 평가하였다. 7 mM ABTS(Sigma-Aldrich, USA)와 2.45 mM potassium persulfate(Sigma-Aldrich, USA)를 최종농도로 혼합(1:1=5 mL:5 mL)하여 50 mL tube에 넣고 호일로 감싼 후 실온에서 24시간 동안 방치였다. 96 well plate에 200 μL를 넣고 734 nm에서 흡광도를 측정한 후 값이 0.7 (±0.05)이 되도록 증류수로 희석하였다. 희석된 ABTS radical 용액 950 μL에 농도별 추출물 50 μL를 가하여 혼합한 후 흡광도의 변화를 위해 10분 후에 734 nm에서 측정하였다.
쌍화 티백 추출액의 세포 독성을 측정하기 위해 MTT assay를 실시하였다. 쌍화 티백 추출액을 회전식 감압농축기(N-1300, Eyela, Tokyo, Japan)를 이용하여 10배 농축한 후 단계별로 희석하여 분석하였다. RAW 264.7 세포를 96 well plate에 5 x 104 cells/well로 분주하고, 37°C, 5% CO2 조건의 배양기에서 24시간 배양하였다. 이후 상층액을 걷어내고 시료를 농도별로 처리한 다음 24시간 반응하였다. 이후 MTT(3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide, Bio basic, Canada)를 처리하고 4시간 반응시켰으며, DMSO(dimethyl sulfoxide, Bio basic, Canada)를 넣고 반응시킨 후 microplate reader를 이용하여 570 nm에서 흡광도를 측정하였다.
농축한 쌍화 티백 추출액을 단계별로 희석하여 NO 생성 억제 활성을 측정하였다. 96 well plate에 세포를 5 × 105 cell/well 농도로 190 μL씩 분주하고, 37°C, 5% CO2 배양기에서 4시간 배양하였다. 세포 분주 4시간 후에 양성 대조물질과 시험물질을 농도별로 5 μL씩 처리하고, 1시간 후에 LPS를 5 μL씩 처리하여 37°C, 5% CO2 배양기에서 24시간 배양하였다. 세포배양액과 Gries 시약(Sigma- Aldrich, USA)을 1:1로 혼합하여 10분 후 microplate reader를 이용하여 540 nm 파장에서 흡광도를 측정하였다.
관능적 품질 평가는 식품공학을 전공하는 대학생 37명을 panel로 선정하여 실험목적, 방법 등을 숙지시킨 후 설문지를 통하여 실시하였다. 관능검사 시간은 오후 3~5시로 하였으며, 시료를 맛본 후 이전 시료의 맛을 제거하기 위해 입을 헹구고, 5분 후에 다음 시료를 평가하도록 하였다. 코팅하지 않은 쌍화 티백과 액상 코팅된 쌍화 티백을 종이컵에 담아 각각 80, 100°C에서 100 mL의 물로 3분간 우려낸 후 관능평가를 실시하였다. 평가 항목은 외관(색), 향, 쓴맛, 떫은 맛, 구수한 맛, 전체적인 기호도의 6가지 항목으로 하였으며, 매우 나쁘다에서 매우 좋다로 하는 7점 척도로 평가하였다.
Ⅲ. 결과 및 고찰
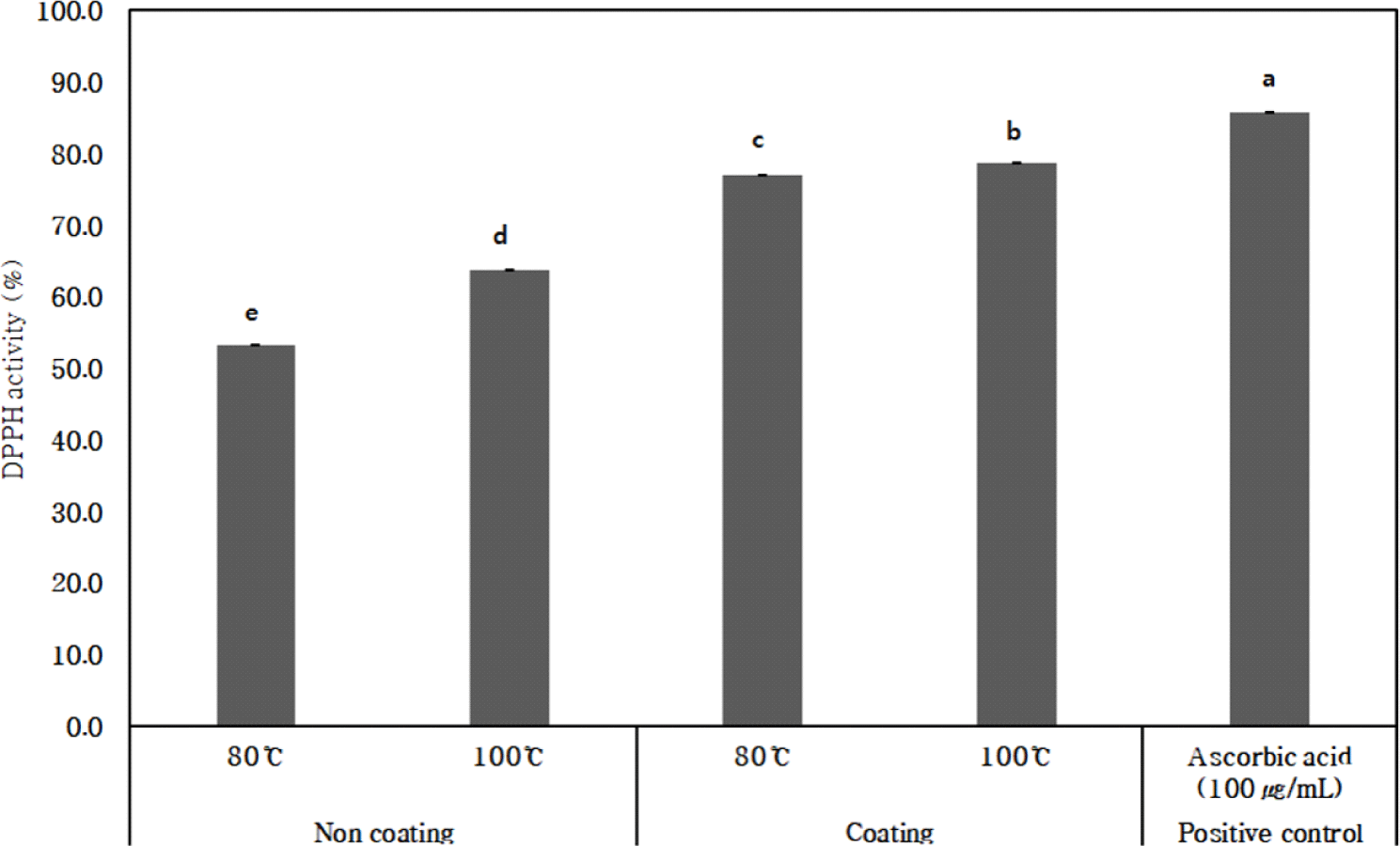
쌍차 티백의 코팅 전후에 대한 DPPH 라디칼 소거 활성을 평가한 결과, 코팅 쌍화 티백을 100°C에서 3분간 추출했을 때 78.66%로 가장 높은 DPPH 라디칼 소거 활성을 보였으며, ascorbic acid 대비 91.70%의 효과를 나타냈다(Fig. 1). 80°C에서 코팅 쌍화 티백의 DPPH 라디칼 소거 활성은 77.03%로 나타났다. 코팅하지 않은 티백의 DPPH 라디칼 소거 활성은 80, 100 °C에서 각각 53.26, 63.65%로 상대적으로 낮은 DPPH 라디칼 소거 활성 값을 보였다. Kim 등(2011)은 전통적 방법과 동일한 구성 약재를 단일로 제조하여 혼합한 쌍화탕의 DPPH 라디칼 소거 활성을 측정한 결과, 동등한 효과를 확인하였다. 약재들이 혼합된 티백 활용 시 편리하게 사용하면서도 개별 약재의 효능이 유지될 수 있음을 시사한다.
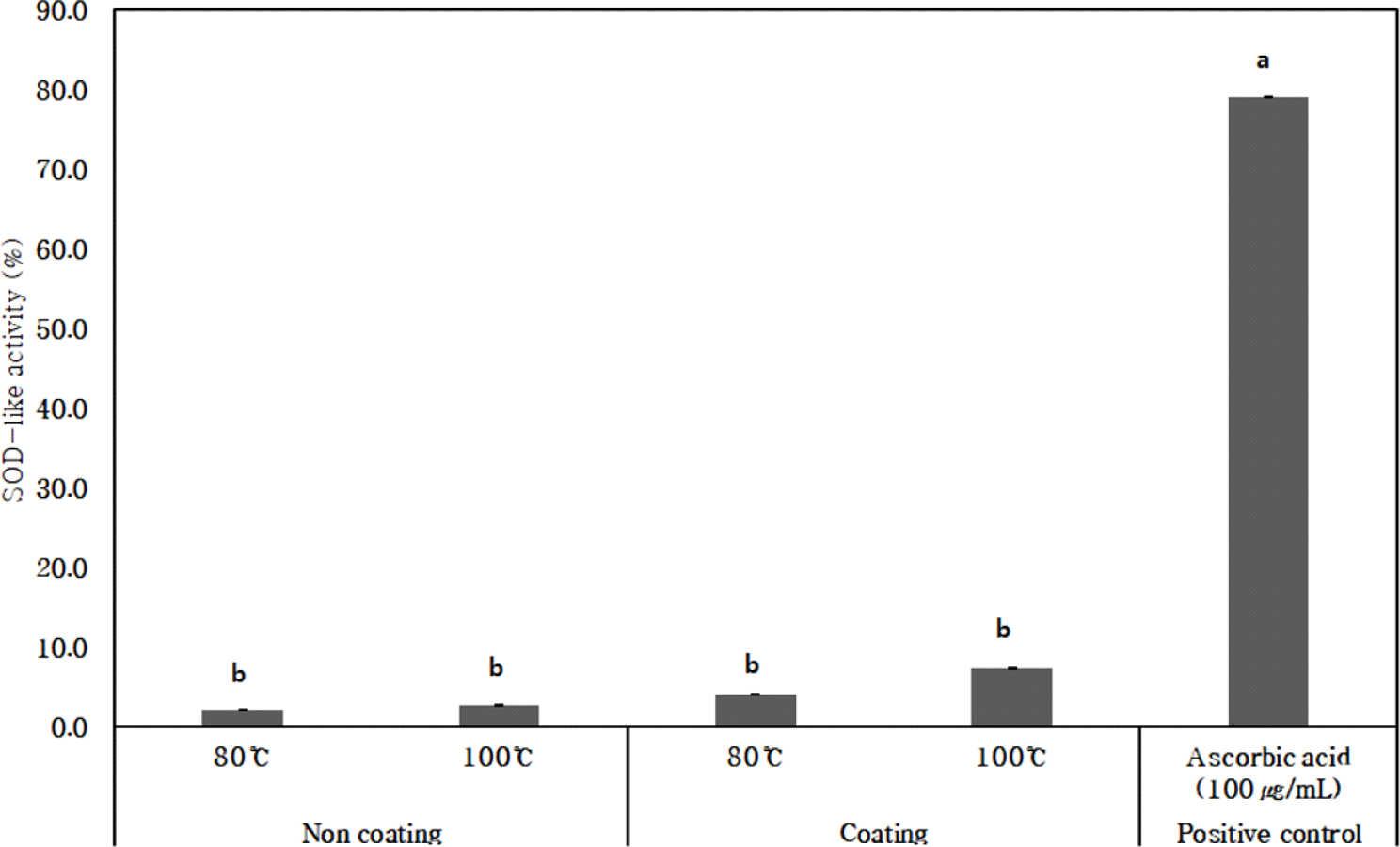
쌍화 티백의 온도에 따른 SOD 유사 활성 측정 결과, ascorbic acid 대비 효과는 낮게 나타났다(Fig. 2). 코팅된 티백을 100°C로 3분간 추출했을 때 7.28%로 SOD 유사 활성이 가장 높았으며, 80°C에서는 4.08%의 SOD 유사 활성을 보였다. 코팅하지 않은 티백은 80, 100°C에서 각각 2.15, 2.65%의 낮은 SOD 유사 활성 값을 보여 DPPH 라디칼 소거 활성과 같이 코팅된 쌍화 티백에서 높게 나타나는 경향을 보였다.
Park 등(2012)은 쌍화탕 추출물의 추출 용매에 따른 SOD 유사 활성을 측정한 결과, 열수 추출과 50% 에탄올 추출 시 용매에 따른 효과의 차이는 없었으며, 10 mg/mL의 농도에서는 40%의 활성 저해 효과가 있다고 보고하였다. 본 연구결과보다는 높은 SOD 유사 활성을 나타냈는데, 이는 쌍화탕 원료의 배합 비율, 추출 조건, 처리 농도의 차이에 의한 것으로 판단된다.
쌍화 티백의 코팅 전후 ABTS 라디칼 소거 활성을 평가한 결과, 코팅된 티백을 100°C로 3분간 추출했을 때 34.33%로 ABTS 라디칼 소거 활성이 가장 높게 나타났다(Fig. 3). 80°C에서는 20.85%의 ABTS 라디칼 소거 활성을 보였다. 코팅하지 않은 티백은 80, 100°C에서 각각 1.74, 3.02%의 낮은 ABTS 라디칼 소거 활성 값을 보였다. Park 등(2017)은 시판 쌍화 음료의 ABTS 라디칼 소거 활성을
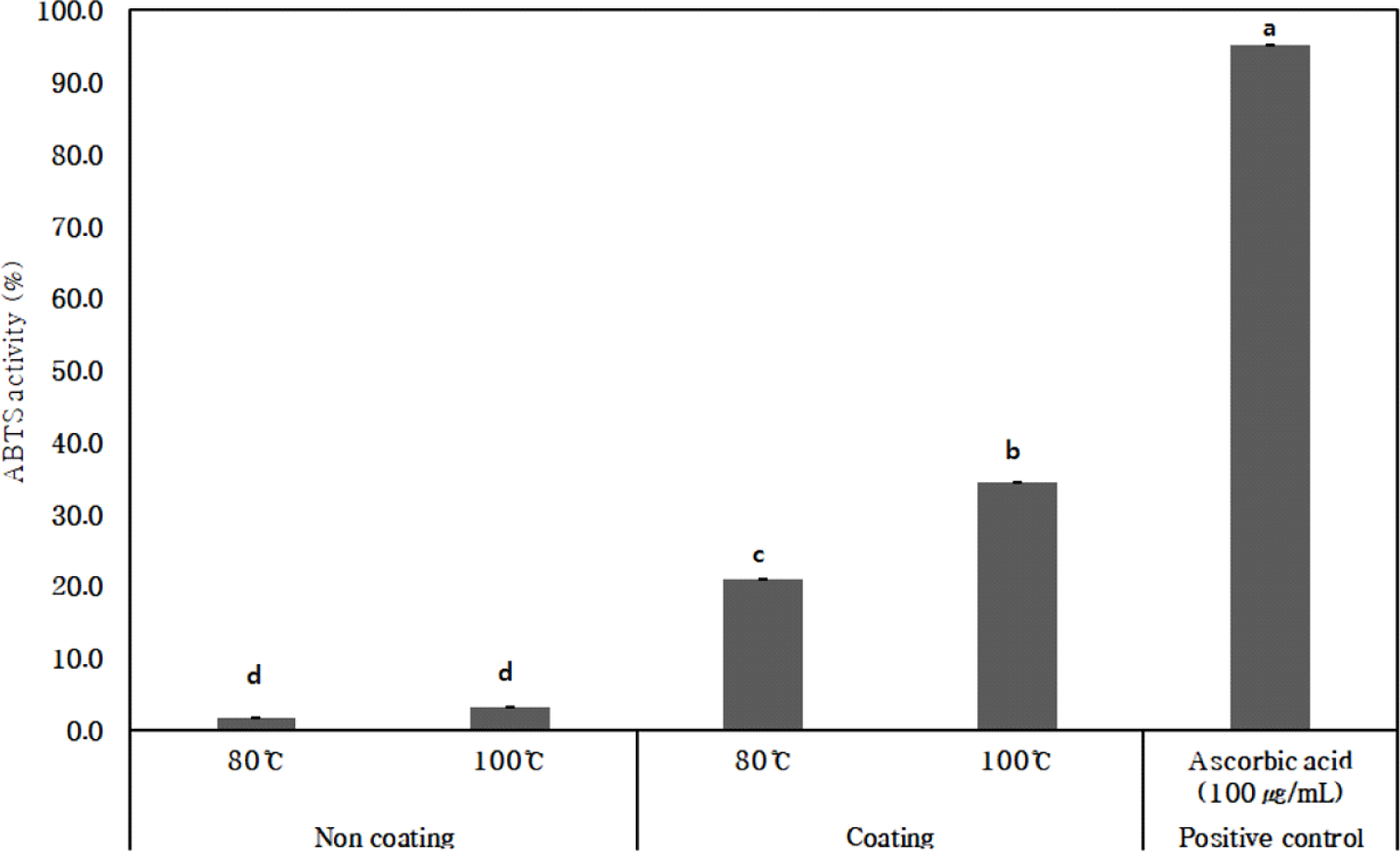
평가한 결과, 22.21%의 소거능이 있다고 보고하였다. 본 연구결과, 쌍화 티백에 추출액 코팅을 통해 기존 음료보다 ABTS radical 소거 활성을 향상시킬 수 있음을 확인하였다.
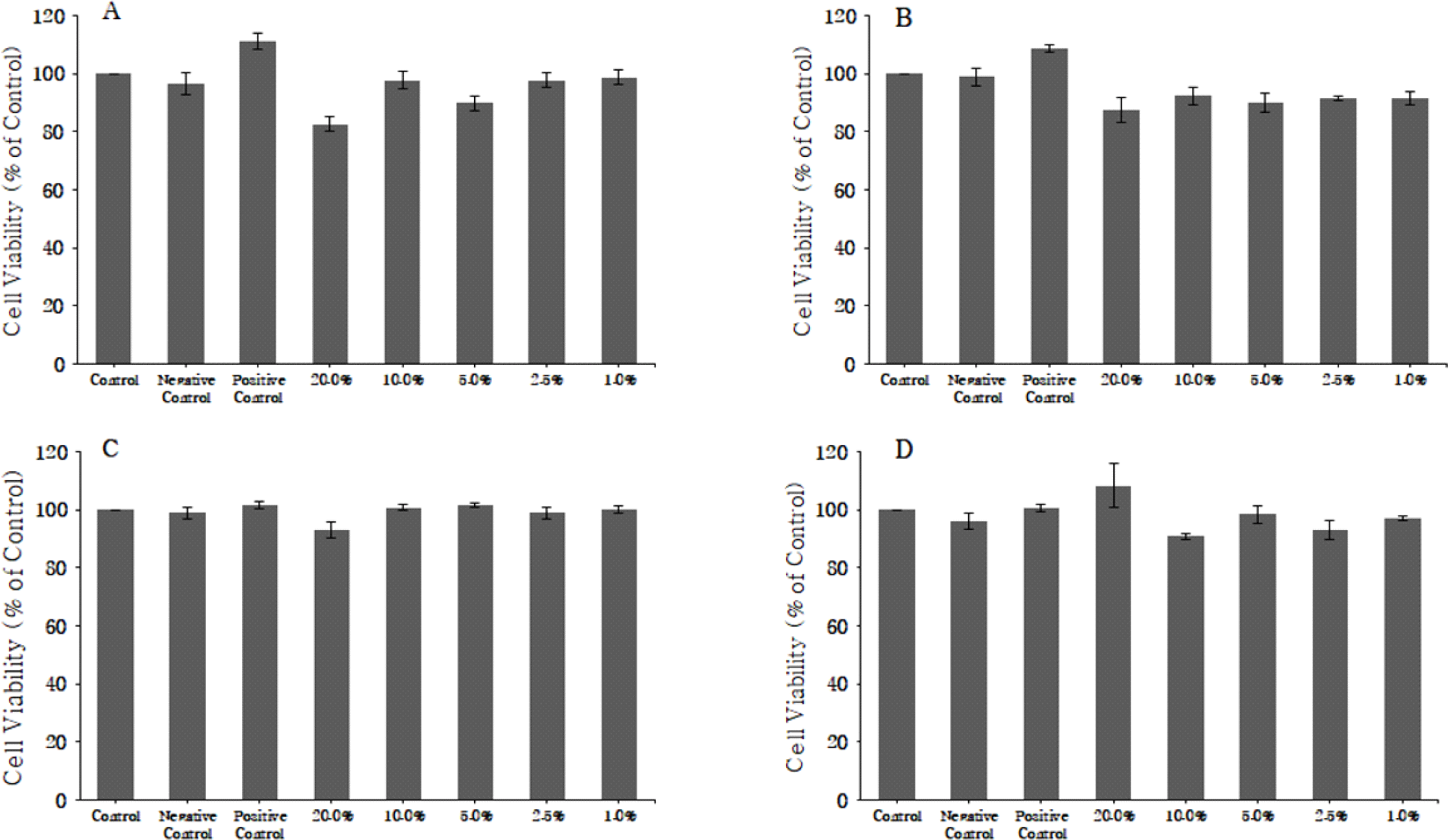
코팅 쌍화 티백과 코팅하지 않은 쌍화 티백을 80, 100°C로 3분간 추출한 후 쌍화 추출액을 10배 농축한 다음 단계별로 1∼20%의 농도로 희석하여 세포 독성을 측정하였다(Fig. 4). 각 티백 추출물을 농도별로 MTT assay를 실시한 결과, 처리 농도 범위에서 세포 독성은 나타나지 않아 세포에 안전한 것으로 평가되었다.
코팅 쌍화 티백과 코팅하지 않은 쌍화 티백을 80, 100°C로 3분간 추출한 후, 추출액을 10배 농축하였다. 농축액을 단계별로 희석하여 NO 생성 억제 활성을 평가한 결과, Fig. 5와 같이 코팅 쌍화 티백을 100°C로 추출한 후 20% 농도로 희석한 시료에서 88.5%로 가장 높게 나타났으며, 10% 희석 농도에서는 73.1%의 NO 생성 억제 활성을 보였다. 80°C로 추출한 후 20% 농도로 희석한 코팅 쌍화 티백 시료에서는 86.1%로 나타났으며, 10% 희석 농도에서는 77.2%의 활성을 보였다. 코팅하지 않은 쌍화 티백을 100°C로 추출한 후 20% 농도로 희석한 시료에서 84.8%로 NO 생성 억제 효과가 나타났으며, 10% 희석 농도에서는 35.1%의 NO 생성 억제 활성을 보였다. 80°C로 추출한 후 20% 농도로 희석한 시료에서는 57.7%로 나타났으며, 10% 희석 농도에서는 21.3%의 NO 생성 억제 활성을 보였다. 코팅한 쌍화 티백에서 NO 생성 억제 효과가 증대됨을 확인하였다.
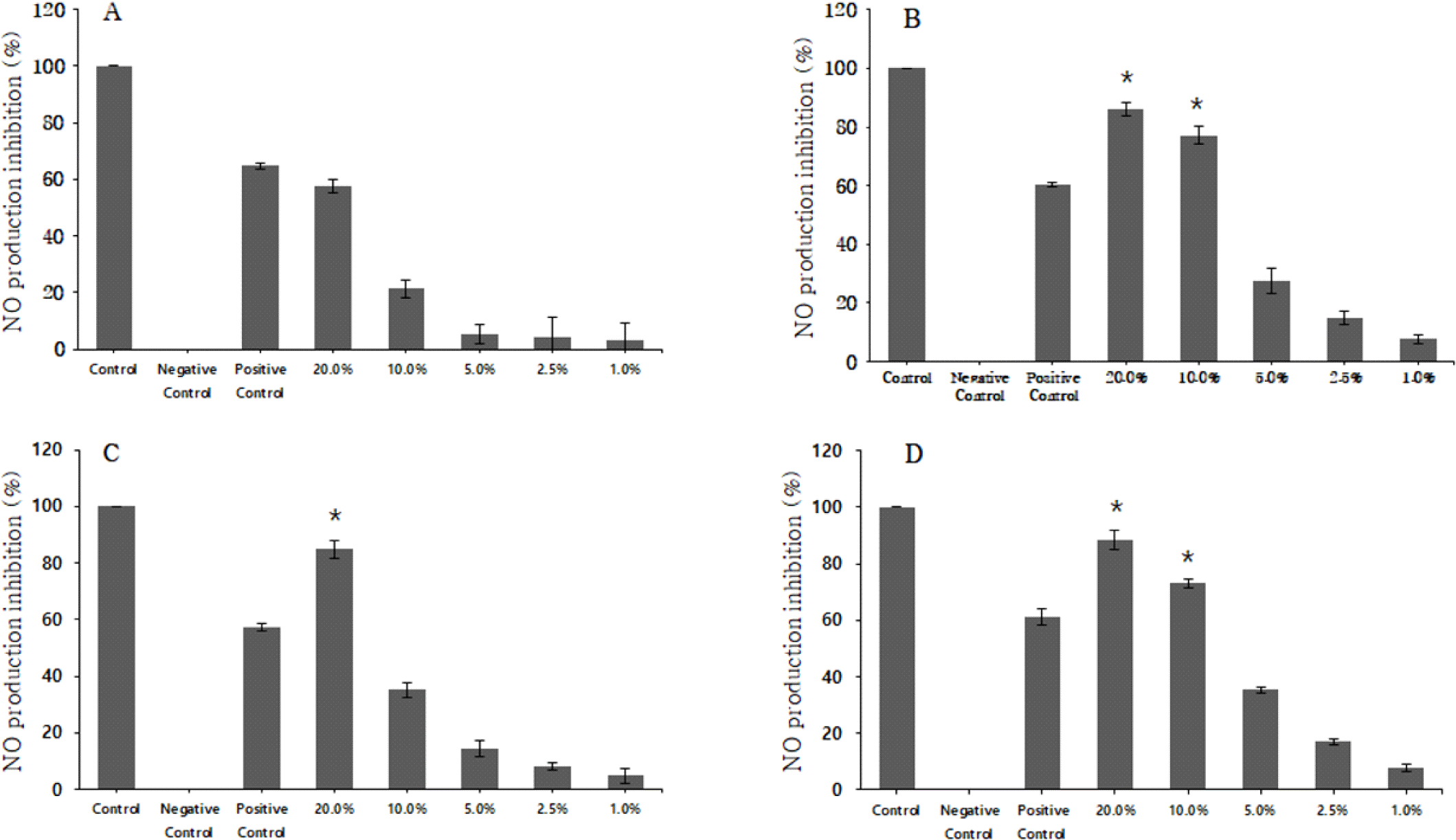
Jung 등(2010)의 연구에 의하면 쌍화탕은 대식세포 증식 효과를 나타내어 항염 효과가 있음을 확인하였다. 또한 흰쥐를 이용한 동물실험 결과, 초기 염증모델과 만성 염증모델에서 부종 억제 효과와 관절염의 소염작용을 통해 항염증 효과를 확인하였다(Kim & Hwang, 1981).
쌍화 티백의 코팅 전후에 대해 37명의 관능평가 결과, 코팅한 쌍화 티백의 색은 5.89로 코팅하지 않은 상화 티백에 비해 좋은 결과를 보였다(Fig. 6). 코팅한 쌍화 티백의 향에서도 5.05로 좋게 나타났으며, 쓴맛과 떫은맛, 구수한 맛은 각각 4.43, 4.46, 5.22로 코팅하지 않은 티백에 비해 좋은 평가 결과를 보였다. 전체적인 기호도를 평가한 결과, 코팅된 쌍화 티백은 4.84로 코팅하지 않는 티백보다 높은 기호도를 보였다. 관능평가 결과, 코팅 쌍화 티백이 모든 항목에서 좋게 평가되어 상품화 가치가 증대 될 수 있음을 확인하였다.
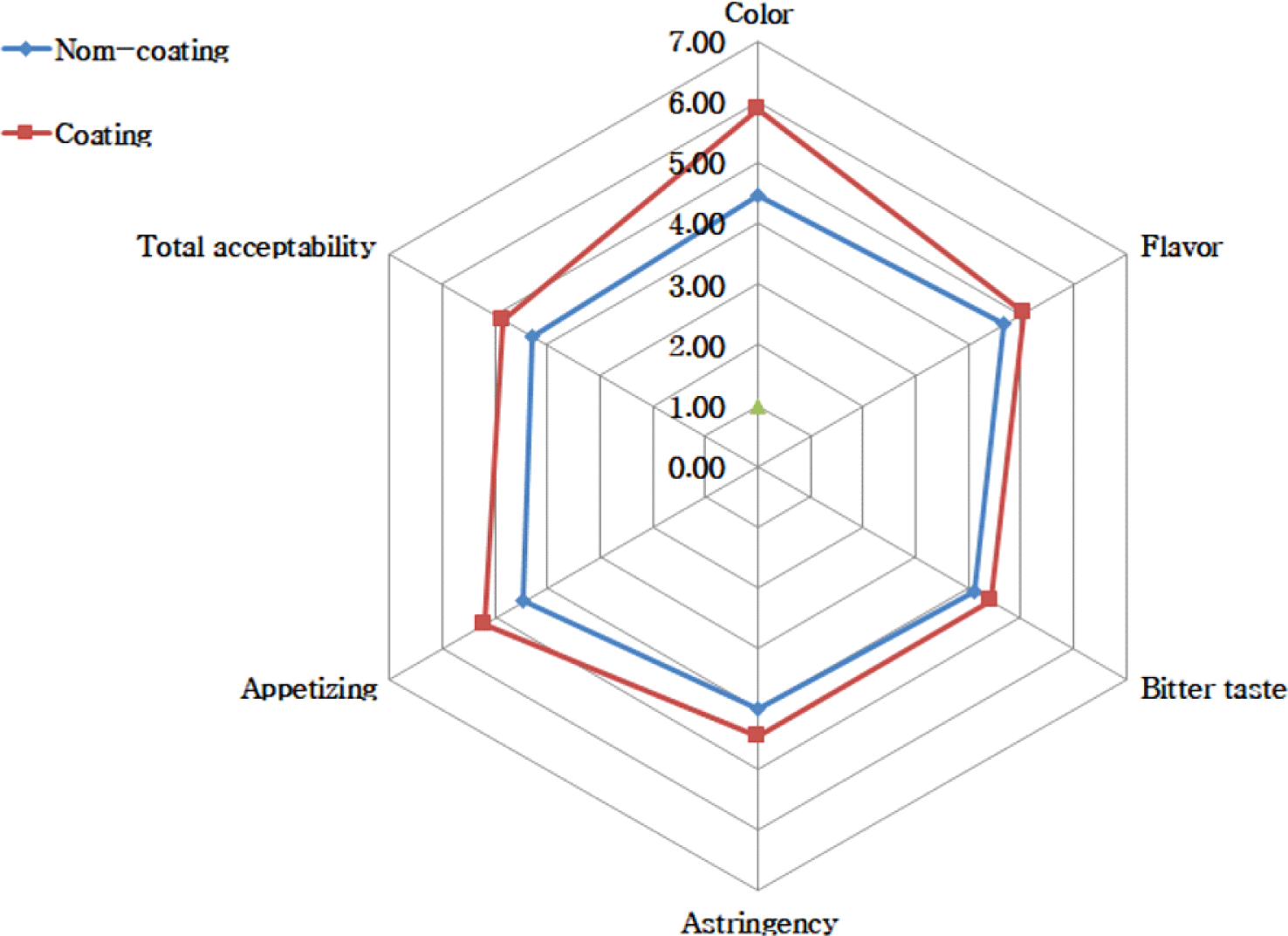
Baek과 Jhee(2008)는 쌍화 음료의 저열량화를 위해 액상과당, 아스파탐, 아세로설팜 칼륨, 효소처리 스테비아의 감미료를 병용 처리하여 관능적 특성을 평가한 결과, 효소처리 스테비아와 아세로설팜 칼륨 혼합사용이 기존 액상과당 사용 쌍화 음료보다 좋은 기호성을 보였다고 보고하였다. 이는 티백 코팅 추출물에 효소처리 스테비아와 아세로설팜 칼륨의 혼합 감미료를 첨가하여 코팅 티백차를 제조할 경우 성상에는 영향을 주지 않으며, 관능적 기호도를 상승시킬 수 있을 것으로 판단된다.
Ⅳ. 요 약
본 연구는 쉽게 이용할 수 있는 쌍화 티백에 쌍화 추출물을 코팅하여 항산화, 항염 및 관능평가에 미치는 효과를 평가하기 위해 수행되었다. 코팅한 쌍화 티백을 100°C에서 3분간 추출 시 DPPH 라디칼 소거 활성, SOD 유사 활성, ABTS 라디칼 소거 활성이 각각 78.66, 7.28, 34.33%로 가장 높은 항산화 효과를 나타냈다. 처리 농도 범위에서 세포 독성은 나타나지 않았으며, 100°C로 3분간 추출한 후 쌍화 추출액을 10배 농축한 다음 단계별로 희석하여 NO 생성 저해 활성을 평가한 결과, 20% 농도로 희석한 시료에서 88.5%로 가장 높게 나타났다. 관능평가 결과, 색, 향, 떫은맛, 구수한 맛, 전체적 기호도에서 코팅하지 않은 쌍화 티백에 비해 코팅한 쌍화 티백에서 좋은 평가 결과를 보였다. 쌍화 티백에 쌍화 추출액을 코팅함으로써 효능이 증대되고, 기호성 향상됨을 확인하였다. 이러한 결과를 통해 쌍화 티백의 상품화 가치를 상승시킬 수 있을 것으로 생각된다.






